肿瘤病因学研究引起肿瘤的始动因素,肿瘤发病学则研究肿瘤的发病机制与肿瘤发生的条件。要治愈肿瘤和预防肿瘤的发生,关键问题是查明肿瘤的病因及其发病机制。
关于肿瘤的病因学和发病学,多年来进行了广泛的研究,虽然至今尚未完全阐明,但近年来分子生物学的迅速发展,特别是对癌基因和肿瘤抑制基因的研究,已经初步揭示了某些肿瘤的病因与发病机制,例如伯基特淋巴瘤和人类T细胞白血病/淋巴瘤。目前的研究表明,肿瘤从本质上说是基因病。引起遗传物质DNA损害(突变)的各种环境的与遗传的致癌因子可能以协同的或者序贯的方式,激活癌基因或(和)灭活肿瘤的抑制基因,使细胞发生转化(transformation)。被转化的细胞可先呈多克隆性增生,经过一个漫长的多阶段的演进过程(progression),其中一个克隆可相对无限制地扩增,通过附加突变,选择性地形成具有不同特点的亚克隆(异质性),从而获得浸润和转移的能力(恶性转化),形成恶性肿瘤。图7-19示肿瘤的病因和发病机制模式。
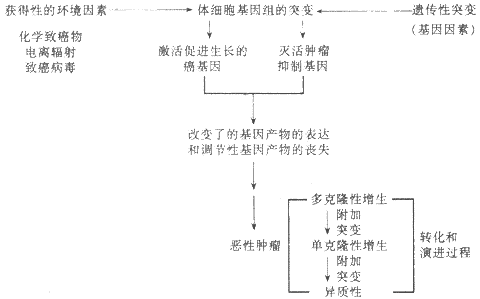
图7-19肿瘤的病因和发病机制模式图(采自Kumar,稍改)
一、肿瘤发生的分子生物学基础
1.癌基因
(1)原癌基因、癌基因及其产物:现代分子生物学的重大成就之一是发现了原癌基因(proto-oncogene)和原癌基因具有转化成致癌的癌基因(oncogene)的能力。Bishop和Varmus因为在这方面的贡献而获得1989年的诺贝尔奖。
癌基因是首先在逆转录病毒(RNA病毒)中发现的。含有病毒癌基因的逆转录病毒能在动物迅速诱发肿瘤并能在体外转化细胞。后来在正常细胞的DNA中也发现了与病毒癌基因几乎完全相同的DNA序列。被称为细胞癌基因。如ras,myc等。由于细胞癌基因在正常细胞中乃以非激活的形式存在,故又称为原癌基因。原癌基因可以由于多种因素的作用使其结构发生改变,而被激活成为癌基因。
原癌基因编码的蛋白质大多是对正常细胞生长十分重要的细胞生长因子和生长因子受体,如血小板衍生生长因子(PDGF)、纤维母细胞生长因子(FGF)、表皮细胞生长因子受体(EGF-R)、重要的信号转导蛋白质(如酪氨酸激酶、丝氨酶-苏氨酸激酶等)以及核调节蛋白(如转录激活蛋白)等。表7-4示常见的癌基因及其产物。
表7-4 几种常见的癌基因及其激活方式和相关的人类肿瘤
| 编码的蛋白质 | 原癌基因 | 激活机制 | 相关人类肿瘤 |
| 生长因子: | |||
| PDGF-β链 | sis | 过度表达 | 星形细胞瘤,骨肉瘤 |
| FGF | hst-1,int-2 | 过度表达 | 胃癌,膀胱癌,乳腺癌 |
| 生长因子受体: | |||
| EGF受体 | erb-B1 | 扩增 | 胶质瘤 |
| EGF样受体 | neu(erb-B2) | 扩增 | 乳腺癌,卵巢癌,肾癌 |
| 信号转导蛋白: | |||
| GTP-结合蛋白 | ras | 点突变 | 多种人体肿瘤,包括肺,结肠,胰,白血病 |
| 酪氨酸激酶 | abl | 易位 | 慢性粒细胞性,急性淋巴细胞性白血病 |
| 核调节蛋白: | |||
| 转录激活蛋白 | myc | 易位 | 伯基特淋巴瘤 |
| N-myc | 扩增 | 神经母细胞瘤,小细胞肺癌 | |
| 线粒体蛋白: | bcl-2 | 易位 | 滤泡性B-细胞淋巴瘤 |
(2)原癌基因的激活:原癌基因在各种环境的或遗传的因素作用下,可发生结构改变(突变)而变为癌基因;也可以是原癌基因本身结构没有改变,而是由于调节原癌基因表达的基因发生改变使原癌基因过度表达。以上基因水平的改变可继而导致细胞生长刺激信号的过度或持续出现,使细胞发生转化。引起原癌基因突变的DNA结构改变包括点突变(如90%的胰腺癌有ras 基因的点突变)、染色体易位(如伯基特淋巴瘤的t(8:14),慢性粒细胞白血病的Phl染色体)、插入诱变、基因缺失和基因扩增(如神经母细胞瘤的N-myc原癌基因可复制成多达几百个拷贝,在细胞遗传学上表现为染色体出现双微小体和均染区)。癌基因编码的蛋白质(癌蛋白)与原癌基因的正常产物相似,但有质或量的不同。通过生长因子或生长因子受体增加、产生突变的信号转导蛋白与DNA结合的转录因子等机制,癌蛋白调节其靶细胞的代谢、促使该细胞逐步转化,成为肿瘤细胞。
2.肿瘤抑制基因 与原癌基因编码的蛋白质促进细胞生长相反,在正常情况下存在于细胞内的另一类基因——肿瘤抑制基因的产物能抑制细胞的生长。若其功能丧失则可能促进细胞的肿瘤性转化。由此看来,肿瘤的发生可能是癌基因的激活与肿瘤抑制基因的失活共同作用的结果。目前了解最多的两种肿瘤抑制基因是Rb基因和P53基因。它们的产物都是以转录调节因子的方式控制细胞生长的核蛋白。其它肿瘤抑制基因还有神经纤维瘤病-1基因、结肠腺瘤性息肉基因、结肠癌丢失基因和Wilms瘤-1等。
(1)Rb基因:Rb基因随着对一种少见的儿童肿瘤——视网膜母细胞瘤的研究而最早发现的一种肿瘤抑制基因。Rb基因的纯合子性的丢失见于所有的视网膜母细胞瘤及部分骨肉瘤、乳腺癌和小细胞肺癌等。Rb基因定位于染色体13q14,编码一种核结合蛋白质(P105-Rb)。它在细胞核中以活化的脱磷酸化和失活的磷酸化的形式存在。活化的Rb蛋白对于细胞从G0/G1期进入S期有抑制作用。当细胞受到刺激开始分裂时,Rb 蛋白被磷酸化失活,使细胞进入S期。当细胞分裂成两个子细胞时,失活的(磷酸化的)Rb蛋白通过脱磷酸化再生使子细胞处于G1期或G0的静止状态。如果由于点突变或13q14的丢失而使Rb基因失活,则Rb蛋白的表达就会出现异常,细胞就可能持续地处于增殖期,并可能由此恶变。
(2)p53基因:p53基因定位于17号染色体。正常的p53蛋白(野生型)存在于核内,在脱磷酸化时活化,有阻碍细胞进入细胞周期的作用。在部分结肠癌、肺癌、乳腺癌和胰腺癌等均发现有p53基因的点突变或丢失,从而引起异常的p53蛋白表达,而丧失其生长抑制功能,从而导致细胞增生和恶变。近来还发现某些DNA病毒,例如HPV和SV-40,其致癌作用是通过它们的癌蛋白与活化的Rb蛋白或p53蛋白结合并中和其生长抑制功能而实现的。
3.多步癌变的分子基础 恶性肿瘤的发生是一个长期的、多因素造成的分阶段的过程,这已由流行病学、遗传学和化学致癌的动物模式所证明。近年来的分子遗传学研究从癌基因和肿瘤抑制基因的角度为此提供了更加有力的证明。单个基因的改变不能造成细胞的完全恶性转化,而是需要多基因的改变,包括几个癌基因的激活和两个或更多肿瘤抑制基因的丧失。以结肠癌的发生为例,在从结肠上皮过度增生到结肠癌的演进过程中,关键性的步骤是癌基因以及肿瘤抑制基因的丧失或突变。这些阶段梯性积累起来的不同基因分子水平的改变,可以在形态学的改变上反映出来(图7-20)。
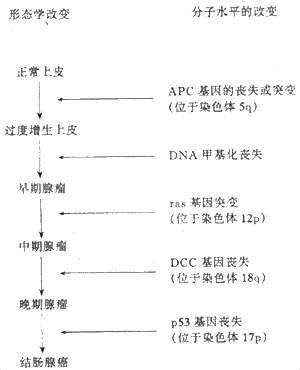
图7-20 结直肠癌通过上皮增生-腺瘤-癌的阶梯性的演进的分子生物学和形态学改变的关系(采自Kumar)
二、环境致癌因素及其致癌机制
1.化学致癌因素 现已确知的对动物有致癌作用的化学致癌物约有1000多种,其中有些可能和人类癌瘤有关。对化致癌物的研究表明:①各种化学致癌物在结构上是多种多样的。基中少数不需在体内进行代谢转化即可致癌,称为直接作用的化学致癌物,如烷化剂。绝大多数则只有在体内(主要是在肝)进行代谢,活化后才能致癌,称为间接作用的化学致癌物或前致癌物,其代谢活化产物称终末致癌物。如3,4-苯并芘是间接致癌物,其终末致癌物是环氧化物;②所有的化学致癌物在化学上都具有亲电子结构的基团,如环氧化物、硫酸酯基团等。它们都与细胞大分子的亲核基团(如DNA分子中的鸟嘌呤的N-7、C-8,腺嘌呤的N-1、N-3,胞嘧啶的N-3等)共价结合,形成加合物,导致DNA的突变。化学致癌物大多数是致突变剂(mutagens);③某些化学致癌物的致癌作用可由其它无致癌作用的物质协同作用而增大。这种增加致癌效应的物质称为促癌物(promoter),如巴豆油、激素、酚和某些药物。致癌物引发初始变化称为激发作用(initiation),而促癌物的协同作用称为促进作用(promotion)。据此,Berenblum(1942)提出致癌过程的第二阶段学说,即激发和促进两个过程。现在认为激发过程是由致癌物引起的不可逆的过程,使得一种原癌基因(如ras基因)突变性活化,这种突变可遗传给子代细胞;促进过程据目前研究,可能是由于促癌剂(如巴豆油)是细胞内信号转导通道的关键性成分——蛋白激酶C的活化剂,并且能使某些细胞分泌生长因子所致。因此促进作用能促使突变的细胞克隆性生长、抑制其正常分化,最后在附加突变的影响下形成恶性肿瘤。此学说在预恶性肿瘤具有现实意义,因为激发过程是很短暂的,大多不可逆转,而促进过程则很长,一般需10~20年。因此,如能减少环境中的促癌因子,亦可有效地预防恶性肿瘤的发生。
主要的化学致癌物质有以下几类:
(1)间接作用的化学致癌物:
1)多环芳烃:存在于石油、煤焦油中。致癌性特别强的有3,4-苯并芘,1,2,5,6-双苯并蒽,3-甲基胆蒽及9,10-二甲苯蒽等。这些致癌物质在使用小剂量时即能在实验动物引起恶性肿瘤,如涂抹皮肤可引起皮肤癌,皮下注射可引起纤维肉瘤等。3,4-苯并芘是煤焦油的主要致癌成分,还可由于有机物的燃烧而产生。它存在于工厂排出的煤烟、烟草点燃后的烟雾中。近几十年来肺癌的发生率之日益增加,公认与吸烟和工业城市严重的大气污染有密切关系。此外,据调查,烟熏和烧烤的鱼、肉等食品中也含有多环芳烃,这可能和某些地区胃癌的发病率较高有一定关系。多环芳烃在肝经细胞色素氧化酶P450系统氧化成环氧化物,后者以其亲电子基因(不饱和的C-C键)与核酸分子以共价健结合而引起突变。
2) 芳香胺类与氨基偶氮染料:致癌的芳香胺类,如乙荼胺、联苯胺、4-氨基联苯等,与印染厂工人和橡胶工人的膀胱癌发生率较高有关。氨基偶氮染料,如以前在食品工业中曾使用过的奶油黄(二甲基氨基偶氮苯,可将人工奶油染成黄色的染料)和猩红,在动物实验可引起大白鼠的肝细胞性肝癌。以上两类化学致癌物主要在肝代谢。芳香胺的活化是在肝通过细胞色素氧化酶P450系统使其N端羟化形成羟胺衍生物,然后与葡萄糖醛酸结合成葡萄糖苷酸从泌尿道排出,并在膀胱水解释放出活化的羟胺而致膀胱癌。
3)亚硝胺类:亚硝胺类物质致癌谱很广,可在许多实验动物诱发各种不同器官的肿瘤。但是近年来引起很大兴趣的主要是可能引起人体胃肠癌或其它肿瘤。亚硝酸盐可作为肉、鱼类食品的保存剂与着色剂进入人体;也可由细菌分解硝酸盐产生。在胃内的酸性环境下,亚硝酸盐与来自食物的各种二级胺合成亚硝胺。我国河南林县的流行病学调查表明,该地食管癌发病率很高与食物中的亚硝胺高含量有关。亚硝胺在体内经过羟化作用而活化,形成有很强的反应性的烷化碳离子而致癌。
4)真菌毒素:黄曲霉菌广泛存在于高温潮湿地区的霉变食品中,尤以霉变的花生、玉米及谷类含量最多。黄曲霉毒素有许多种,其中黄曲霉毒素B1(aflatoxin B1)的致癌性最强,据估计其致癌强度比奶油黄大900倍,比二甲基亚硝胺大75倍,而且化学性很稳定,不易被加热分解,煮熟后食入仍有活性。黄曲霉毒素B1的化学结构为异环芳烃,在肝通过肝细胞内的混合功能氧化酶氧化成环氧化物而致突变。这种毒素主要诱发肝细胞性肝癌。我国和南非肝癌高发区的调查都显示黄曲霉毒素B1在食物中的污染水平与肝癌的发病率有关。但这些地区同时也是乙型肝炎病毒(HBV)感染的高发区。在HBV感染与黄曲霉毒素B1污染之间的关系方面,分子生物学的研究表明,黄曲霉毒素B1的致突变作用是使肿瘤抑制基因p53发生点突变而失去活性,而HBV感染所致的肝细胞慢性损伤和由此引起的肝细胞持续再生为黄曲霉毒素B1的致突变作用提供了有利的条件。因此HBV感染与黄曲霉毒素B1的协同作用是我国肝癌高发地区的主要致癌因素。此外,也已证明,在我国食管癌高发地区居民食用的酸菜中分离出的白地霉菌,其培养物有促癌或致癌作用。
(2)直接作用的化学致癌物:这类化学致癌物不需要体内代谢活化即可致癌,一般为弱致癌剂,致癌时间长。
1)烷化剂与酰化剂:例如抗癌药中的环磷酰胺、氮芥、本丁酸氮芥、亚硝基脲等。这类具有致癌性的药物可在应用相当长时间以后诱发第二种肿瘤,如在化学治疗痊愈或已控制的白血病、何杰金淋巴瘤和卵巢癌的病人,数年后可能发生第二种肿瘤,通常是粒细胞性白血病。某些使用烷化剂的非肿瘤病人,如类风湿性关节炎和Wegener肉芽肿的病人,他们发生恶性肿瘤的机率大大高于正常人。因此这类药物应谨慎使用。
2)其它直接致癌物:金属元素对人类也有致癌的作用,如镍、铬、镉、铍等,如炼镍工人中,鼻癌和肺癌明显高发;镉与前列腺癌、肾癌的发生有关;铬可引起肺癌等。其原因可能是金属的二价阳离子,如镍、镉、铅、铍、钴等,是亲电子的,因此可与细胞大分子,尤其是DNA反应。例如镍的二价离子可以使多聚核苷酸解聚。一些非金属元素和有机化合物也有致癌性,如砷可诱发皮肤癌;氯乙烯可致塑料工人的肝血管肉瘤;苯致白血病等,也受到关注。
化学致癌大多与环境污染和职业因素有关,因此彻底治理环境污染,防治职业病,对于减少恶性肿瘤的发病是极其重要的。目前发现的具有防癌或抗癌作用的稀有元素有钼、硒、镁、铂等。表7-5列出主要的化学致癌物、易感人群和诱发的肿瘤。
表7-5 主要的化学致癌物及易感人群和诱发的肿瘤
| 化学致癌物 | 易感人群 | 诱发的主要肿瘤 |
| 直接作用的 | ||
| 烷化剂 | 接受化学治疗的恶性肿瘤病人 | 白血病 |
| 间接作用的 | ||
| 多环芳烃 | 吸烟者、食用熏制鱼肉者 | 肺癌、胃癌 |
| 芳香胺 | 染料工人、橡胶工人 | 膀胱癌 |
| 亚硝胺 | 亚硝酸盐污染食物的食用者 | 食管癌、胃癌 |
| 黄曲霉毒素B1 | 污染食物的食用者 | 肿细胞性肿癌 |
| 石棉纤维 | 矿工、接触者 | 肺癌、胸膜间皮瘤 |
| 氯乙烯 | 塑料厂工人 | 肝血管肉瘤 |
| 苯 | 橡胶工人、染料工人 | 白血病 |
| 砷 | 矿工、农药工人和喷撒者 | 皮肤癌、肺癌、肝癌 |
| 镍 | 炼镍工人 | 鼻癌、肺癌 |
| 铬 | 接触含铬气体者 | 鼻癌、肺癌、喉癌 |
| 镉 | 接触者 | 前列腺癌、肾癌 |
2.物理性致癌因素 已证实的物理性致癌因素主要是离子辐射。异物、慢性炎性刺激和创伤亦可能与促癌有关。
(1)电离辐射:包括X射线、γ射线、亚原子微粒(β粒子、质子、中子或α粒子)的辐射以及紫外线照射。大量事实证明,长期接触X射线及镭、铀、氡、钴、锶等放射性同位素,可以引起各种不同的恶性肿瘤,例如放射工作者长期接触X射线而又无必要的防护措施时,常可发生手部放射性皮炎以致皮肤癌;其急性和慢性粒细胞性白血病的发生率亦较一般人高10倍以上。在出生前或出生后接受过X线照射的儿童,其急性白血病的发生率高于一般儿童。开采含放射性物质(钴、氡等)的矿工易患肺癌。日本长崎、广岛在第二次世界大战时受原子弹爆炸影响的幸存居民,经过长期观察,发现慢性粒细胞白血病的发生率明显增高(照射后4~8年为发病高峰),甲状腺癌、乳腺癌、肺癌等的发生率亦较高。在婴幼儿期接受过颈部放射线照射者,甲状腺癌发生率明显增高。有些放射性同位素如32P、48Sr、210Po、239Pu等摄入能诱发骨肉瘤。
辐射能使染色体断裂、易位和发生点突变,因而激活癌基因或者灭活肿瘤抑制基因。由于与辐射有关的肿瘤的潜伏期较长,因此肿瘤最终可能当辐射所损伤的细胞的后代又受到其它环境因素(如化学致癌剂、病毒等)所致的附加突变之后,才会出现。
动物实验和临床观察均证实,阳光中紫外线长期过度照射可引起外露皮肤的鳞状细胞癌、基底细胞癌和恶性黑色素瘤。白种人或照射后色素不增加的有色人种最易发生。其作用机制是细胞内DNA吸收了光子,使其中相邻的两个嘧啶连接(包括胸腺嘧啶与胸腺嘧啶、胸腺嘧啶与胞嘧啶、胞嘧啶与胞嘧啶),形成嘧啶二聚体。二聚体又形成环丁烷,从而破坏DNA双螺旋中二聚体所在处的磷酸二酯骨架,妨碍DNA分子的复制。在正常人这种损害通常可为一系列DNA修复酶所修复,因此皮肤癌发病少见。而一种罕见的常染色体隐性遗传病——着色性干皮病(xeroderma pigmentosum)的患者,由于先天性缺乏修复DNA所需的酶,不能将紫外线所致的DNA的损害修复,皮肤癌的发病率很高。
(2)热辐射的促癌作用:克什米尔人冬季习惯用怀炉取暖,有时在腹部引起“怀炉癌”;我国西北地区居民冬季烧火取暖,有时臀部皮肤发生癌变形成所谓“炕癌”。这些说明长期的热辐射可能有一定的促癌作用。在烧伤瘢痕的基础上易发生“瘢痕癌”,有人在烧伤瘢痕中发现化学致癌物。
(3)慢性炎性刺激:肿瘤必须在细胞增生的基础上发生。慢性炎症时产生的细胞生长因子能使细胞持续增生,在此基础上DNA易发生突变而发生肿瘤。因而慢性刺激有促癌作用。慢性皮肤溃疡、结石引起的慢性胆囊炎、慢性子宫颈炎和子宫内膜增生等病变有时可发生癌变,可能即与此有关。
(4)异物:石棉和石棉制品能导致人的胸膜间皮瘤,重度暴露于石棉纤维的工人,其胸膜间皮瘤的发生率可达2%~3%,潜伏期一般为20年。动物实验证明,植入动物体内的异物,如塑料、金属片,玻璃纤维等,可以诱发各种肉瘤。肿瘤的发生与植入物体的化学性关系不大而与物体表面的形状、光滑程度和耐久性有关。人类对于异物刺激有较大的耐受性,虽然尚无植入塑料和金属致癌的报道,但是已人工乳房(有机硅橡胶制成)与乳腺癌有关的报告。
另一种与肿瘤有关的异物是寄生虫。医学文献中早就有埃及血吸虫感染的病人,其膀胱癌的发生率高于正常人的报告。在我国,日本血吸虫
■[此处缺少一些内容]■
RNA病毒(逆转录病毒)的研究导致了癌基因的发现,并由此开创了肿瘤的分子遗传学。在人类已知的与肿瘤有关的病毒并不多。
(1)RNA致瘤病毒:对动物逆转录病毒致癌的研究发现,由于病毒类型的不同,它们是通过转导(transduction)或插入突变(insertional mutagenesis)这两种机制将其遗传物质整合到宿主细胞DNA中,并使宿主细胞分生转化的。①急性转化病毒:这类病毒含有从细胞的原癌基因转导的病毒癌基因,如src,abl,myb等,这些病毒感染细胞后,将以其病毒RNA为模板通过逆转录酶合成的DNA片断整合(integration)到宿主的DNA链中并表达,导致细胞的转化;②慢性转化病毒:这类病毒(如鼠乳腺癌病毒)本身并不含有癌基因,但是有促进基因,当感染宿主细胞后促进基因也可由于逆转录酶的作用而插入到宿主细胞DNA链中的原癌基因附近,引起正常的或突变的原癌基因激活并且过度表达,使宿主细胞转化。
人类T细胞白血病/淋巴瘤病毒I(human T-cell leukemia/lymhoma virus I,HTVL-1)是与人类肿瘤发生密切相关的一种RNA病毒,与主要流行于日本和加勒比地区的T细胞白血病/淋巴瘤有关。HTLV-1病毒与AIDS病毒一样,转化的靶细胞是CD4+的T细胞亚群(辅助T细胞)。HTLV-1在人类是通过性交、血液制品和哺乳传播的。受染人群发生白血病的机率为1%,潜伏期为20~30年。HTLV-1转化T细胞的机制还不甚清楚。HTLV-1不含有任何已知的癌基因,也未发现其在某一原癌基因附近的固定的整合位置。HTLV-1的转化活性与其RNA中的一个称为Tax的基因有关。Tax的产物对病毒的复制十分重要,因其通过对5’-长末端重复片段(5’-long terminal repeat region,5’-LTR)的作用刺激病毒mRNA的转录。Tax蛋白也可激活几种能引起T细胞增生的宿主基因的转录,如编码调节细胞内其它基因表达的P55蛋白c-fos基因,编码PDGF的c-sis基因,编码IL-2及其受体的基因和髓样生长因子(即粒-单核细胞集落刺激因子,GM-CSF)的基因。IL-2及其受体的基因激活后可以建立起一个自分泌体系(autocrine system)能直接引起T细胞的增生;GM-CSF作用于巨噬细胞,使其产生IL-1,从而引起T细胞的增生。因此HTLV-1是通过Tax基因转化细胞的。这些增生的T细胞最初是多克隆性的,而且出现二次突变的可能性大大增加,如其中的某一个发生第二次突变,将导致单克隆性的T细胞肿瘤。
(2)DNA致瘤病毒:DNA病毒中有50多种可引起动物肿瘤。对它们的研究,尤其是对多瘤病毒的研究,提示了DNA病毒致癌的机制。DNA病毒感染细胞后出现两种后果:①如果病毒DNA未能被整合到宿主的基因组中,病毒的复制不会受到干扰,大量的病毒复制最终使细胞死亡;②要引起细胞的转化,病毒基因必需整合到宿主的DNA中并且作为细胞的基因加以表达。多瘤病毒的T基因编码的蛋白质T抗原具有酪氨酸激酶活性,能像生长因子受体那样刺激细胞DNA合成,并使细胞持续增生,而后形成肿瘤。与人类肿瘤发生密切有关的DNA病毒有以下三种:
1)人类乳头状瘤病毒(human papilloma virus,HPV):HPV与人类上皮性肿瘤,主要是与子宫颈和肛门生殖器区域的鳞状细胞癌的关系,近年来已有大量资料予以证实。HPV的某些亚型(如16、18型)的DNA序列已在75%~100%的宫颈癌病例的癌细胞中发现。HPV的致癌机制还不完全清楚。近来发现HPV的16、18和31高危亚型的早期病毒基因产物E6和E7蛋白,极易与Rb和p53基因的产物结合并中和其抑制细胞生长的功能。在体外,Rb和p53基因产物的失活能使人类棘细胞转化并且长期存活,但不形成肿瘤。这时如果再转染一个突变的ras基因,就会引起完全的恶性转化。这说明HPV在致癌时不是单独作用的,需要环境因素的协同。
2)Epstein-Barr病毒(EBV):与之有关的人类肿瘤是伯基特淋巴瘤和鼻咽癌。
伯基特淋巴瘤是一种B细胞性的肿瘤。流行于非洲东部和散发于世界各地。在流行地区,所有病人的瘤细胞都携带EBV的基因组成分并且出现特异的染色体易位t(8:14)。EBV对B细胞有很强的亲和性,能使受染的B细胞发生多克隆性的增生。在正常的个体这种增生是可以控制的,受染者没有症状或者临床表现为自限性的传染性单核细胞增生症。而在非洲流行区,由于疟疾或其它感染损害了患者的免疫功能,受染B细胞乃持续增生。在此基础上如再发生附加的突变(如t(8:14)),则后者使c-myc激活,导致进一步的生长控制丧失,并在其它附加基因损伤的影响下,最终导致单克隆性的肿瘤出现。
鼻咽癌在我国南方和东南亚流行,EBV的基因组也在几所有肿瘤细胞中发现。但是与伯基特淋巴瘤一样,EBV在鼻咽癌发生中的作用也需要其它因素的配合。
3)乙型肝炎病毒(hepatitis b virus,HBV):流行病学调查发现,慢性HBV感染与肝细胞性肝癌的发生有密切的关系。但是HBV本身并不含有可以编码任何转化蛋白(癌蛋白)的基因,其中肝细胞DNA中的整合也没有固定的模式。HBV的致癌作用看来是多因素的:①如在前文所述,HBV导致的慢性肝损伤使肝细胞不断再生,这使另外的致癌因素(如黄曲霉毒素B1)的致突变作用容易发生;②HBV可能编码一种称为X蛋白的调节成分,使受染肝细胞的几种原癌基因激活;③在某些病人,HBV的整合可导致p53基因的失活。由此可见,肝细胞性肝癌的发生也可能是多步骤的。
三、影响肿瘤发生、发展的内在因素及其作用机制
肿瘤发生和发展是一个十分复杂的问题,除了外界致癌因素的作用外,机体的内在因素也起着重要作用,后者包括宿主对肿瘤反应,以及肿瘤对宿主的影响。这些内在因素是复杂的,许多问题至今尚未明了,还有待进一步研究。机体的内在因素可分为以下几方面;
1.遗传因素 人类肿瘤是否有遗传性,以及遗传因素在人类肿瘤的发生上究竟起多大的作用?这是人们普遍关注并不断深入研究的课题。根据一些高癌家族系谱的分析,有以下几种不同情况:
(1)呈常染色显性遗传的肿瘤:如视网膜母细胞瘤、肾母细胞瘤、肾上腺或神经节的神经母细胞瘤等。一些癌前疾病,如结肠多发性腺瘤性息肉症、神经纤维瘤病等本身不是恶性肿瘤,但恶变率极高,有100%的结肠家族性多发性腺瘤性息肉病的病例在50岁以前发生恶变,成为多发性结肠腺癌。这些肿瘤和癌前疾病都属单基因遗传,以常染色体显性遗传的规律出现。其特点为早年(儿童期)发病,肿瘤呈多发性,常累及双侧器官。
(2)呈常染色体隐性遗传的遗传综合征:如患Bloom综合征(先天性毛细血管扩张性红斑及生长发育障碍)时易发生白血病及其他恶性肿瘤;毛细血管扩张性共济失调症患者多发生急性白血病和淋巴瘤;着色性干皮病患者经紫外光照射后易患皮肤基底细胞癌、磷状细胞癌或黑色素瘤。这些肿瘤易感性高的人常伴有某种遗传缺陷,如免疫缺陷、染色体缺陷和内切酶等的缺陷。
(3)遗传因素与环境因素在肿瘤发生中起协同作用,而环境因素更为重要,决定这类肿瘤的遗传因素是属于多基因的。目前发现不少常见肿瘤有家族史,如乳腺癌、胃肠癌、食管癌、肝癌、鼻咽癌、白血病、子宫内膜癌、前列腺癌、黑色素瘤等。
总的说来不同的肿瘤可能有不同遗传传递方式,真正直接遗传的只是少数不常见的肿瘤。遗传因素在大多数肿瘤发生中的作用是对致癌因子的易感性或倾向性。Kundson(1974)提出二次突变假说(two hit hypothesis)来解释遗传性损害在肿瘤发生中作用。以现代分子生物学的术语来描述这一假说是:以视网膜母细胞瘤例,Rb基因定位于染色体13q14,只有两条同源染色体上的Rb等位基因都被灭活,即需经两次突变后,才能使肿瘤发生。在家族性视网膜母细胞瘤患儿基因组中已经存在一个从父母得到的有缺陷的Rb基因拷贝,另一个Rb基因拷贝正常的(杂合型),因而只要再有一次体细胞突变,即可形成肿瘤(纯合型)。这种家族性视网膜母细胞瘤的患儿年龄小,双侧发病的较多。而在散发性的视网膜母细胞瘤的患儿,由于其两个正常的Rb等位基因都要通过体细胞突变而失活才能发病,故出现这种病例的可能性只有家族性的万分之一,而且发病较晚,多为单侧。
2.宿主对肿瘤的反应——肿瘤免疫恶性转化是由于遗传基因的改变引起的。有些异常基因表达的蛋白可引起免疫系统的反应,从而使机体能消灭这些“非已”的转化细胞。如果没有这种免疫监视机制,则肿瘤的发生要比实际上出现的多得多。关于肿瘤免疫的研究不仅对肿瘤的发生有重要的意义。而且为肿瘤的免疫治疗指出了方向。
(1)肿瘤抗原:引起机体免疫反应的肿瘤抗原可分为两类:①只存在于肿瘤细胞而不存在于正常细胞的肿瘤特异性抗原;②存在于肿瘤细胞和某些正常细胞的肿瘤相关抗原。
尽管在肿瘤特异性抗原的研究上花费了大量的时间和精力,企图寻找某种肿瘤的特异性抗原。但是现已在化学致癌的动物模型中发现,肿瘤特异性抗原是个体独特的,即不同个体中同一种致癌物诱发的同一组织学类型的肿瘤有不同的特异性抗原。因此用检测某种肿瘤特异性抗原来诊断或用某抗体来治疗某些肿瘤的可能性在目前尚不存在。肿瘤特异性抗原的个体独特性的原因是,癌变时癌基因发生突变的随机性引起异常蛋白的随机出现,因而无法产生特定的针对某一类肿瘤的抗原。
肿瘤相关抗原在肿瘤中的表达,推测与遗传因素的改变有关。它们又可分为两类:肿瘤胚胎抗原和肿瘤分化抗原。前者在正常情况下出现在发育中的胚胎组织而不见于成熟组织,但可见于癌变组织。例如在胚胎肝细胞和肝细胞性肝癌中出现的甲胎蛋白以及在胚胎组织和结肠癌中出现的癌胚抗原。后者是指肿瘤细胞具有的与分化程度有关的某些抗原。例如前列腺特异抗原见于正常前列腺上皮和前列腺癌细胞。肿瘤相关抗原在有关肿瘤的诊断上是有用的标记,也可用此制备抗体,用于肿瘤的免疫治疗。
(2)抗肿瘤的免疫效应机制:肿瘤免疫反应以细胞免疫为主,体液免疫为辅。参加细胞免疫的效应细胞主要有细胞毒性T细胞(CTL)、自然杀伤细胞(NK)和巨噬细胞。抗肿瘤免疫的机制如图7-21所示。CTL被白细胞介素2(IL-2)激活后可以通过其T细胞受识别瘤细胞上的人类主要组织相容性复合体(major histocompatibility compolex,MHC)I型分子而释放某些溶解酶将瘤细胞杀灭。CTL的保护作用在对抗病毒所致的肿瘤(如EBV引起的伯基特淋巴瘤和HPV导致的肿瘤)时特别明显。NK细胞是不需要预先致敏的、能杀伤肿瘤细胞的淋巴细胞。由IL-2激活后,NK细胞可以溶解多种人体肿瘤细胞,其中有些并不引起T细胞的免疫反应,因此NK细胞是抗肿瘤免疫的第一线的抵抗力量。NK细胞识别靶细胞的机制可能是通过NK细胞受体和抗体介导的细胞毒作用(antibody-dependent cellular cytotoxicity,ADCC)。巨噬细胞在抗肿瘤反应中是与T细胞协同作用的:T细胞产生的α-干扰素可激活巨噬细胞,而巨噬细胞产生的肿瘤坏死因子(TNF-α)和活性氧化代谢产物在溶解瘤细胞中起主要作用。此外巨噬细胞的Fc受体还可与肿瘤细胞表面的IgG结合,通过ADCC杀伤肿瘤细胞。体液免疫参加抗肿瘤反应的机制主要是激活补体和介导NK细胞参加的ADCC。
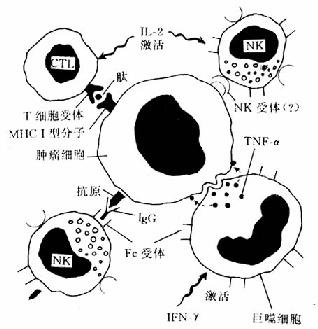
图7-21 抗肿瘤免疫的细胞效应机制
CTL:细胞毒性T淋巴细胞 NK:自然杀伤细胞 IFN-γ:γ-干扰素 TNF-α:肿瘤坏死因子α IL-2:白细胞介素2 MHCI:主要组织相容性复合体Ⅰ型分子
(3)免疫监视:免疫监视机制在抗肿瘤中的作用的最有力的证据是,在免疫缺陷病患者和接受免疫抑制治疗的病人中,恶性肿瘤的发病率明显增加。先天性免疫缺陷病(如X-性联无γ球蛋白血症)的病人有5%发生恶性肿瘤,这比对照组高出200倍。在器官移植的受者和AIDS患者中发生淋巴瘤的可能也大大增加。恶性肿瘤患者随着病程的发展和病情恶化每伴有免疫功能普遍下降,这在晚期患者尤为突出。相反,有些肿瘤,如神经母细胞瘤、恶性黑色素瘤和绒毛膜上皮癌等肿瘤患者,由于机体免疫功能增高,肿瘤可发生自发消退。但大多数恶性肿瘤乃发生于免疫功能正常的人群,这些肿瘤能逃脱免疫系统的监视并破坏机体的免疫系统,其机制还不甚清楚,可能与下列因素有关:①在肿瘤生长过程中,具有较强抗原性的亚克隆被免疫系统消灭,而无抗原性的或者抗原性弱的亚克隆则生长成肿瘤;②CTL攻击肿瘤细胞时要识别瘤细胞膜上的Ⅰ型MHC抗原,故肿瘤细胞MHC抗原表达的丧失或减少,会使瘤细胞避开CTL的攻击;③许多致癌因素同时也抑制宿主的免疫反应,如化学致癌物和电离辐射等;④肿瘤产物也可以抑制免疫反应,如由许多肿瘤分泌的转化生长因子β(TGF-β)就是一种潜在免疫抑制剂;⑤肿瘤引发的有些免疫反应,如抑制性T细胞的激活,本身就可抑制对肿瘤的免疫反应。
(4)肿瘤的免疫治疗:免疫治疗旨在通过替换免疫系统中的受到抑制的成分,或者刺激内源性的反应来增加机体的抗肿瘤能力。目前有三种主要的方法。①继承性细胞治疗:先将病人的周围血淋巴细胞与IL-2一起孵育,然后将产生的淋巴激肽激活杀伤细胞(lymphokine-activated killer cell,LAK细胞,主要由NK细胞组成)再输回病人;或者将从病人切除的肿瘤组织中的淋巴细胞(主要是CTL)在体外与IL-2一起培养后再输回病人。这两种治疗方法的效果还有待于评价;②细胞激肽治疗:主要是用IL-1,IFN-α、γ、TNF-α等细胞激肽与其它治疗方法一起用于抗癌,目前疗效最好的是INF-α对毛细胞白血病的治疗;③抗体治疗:目前的兴趣集中在用抗肿瘤相关抗原的单克隆抗体与细胞毒素结合后制成的“免疫毒素”来治疗肿瘤,这种“魔弹”的疗效正在观察中。
3.其它与肿瘤发病学有关的因素
(1)内分泌因素:内分泌紊乱与某些器官肿瘤的发生发展有密切的关系,如乳腺癌的发生发展可能与患者体内雌激素水平过高或雌激素受体的异常有关。乳腺癌在妊娠期和哺乳期发展得特别快,切除卵巢或用雌激素治疗可使肿瘤明显缩小。此外,激素与恶性肿瘤的转移及扩散也有一定的关系,如垂体前叶激素可促进肿瘤的生长和转移;肾上腺皮质激素对某些造血系统的恶性肿瘤有抑制其生长和转移的作用。
(2)性别和年龄因素:肿瘤的发生在性别上有很大的差异,除生殖器官肿瘤及乳腺癌在女性明显较多见外,胆囊、甲状腺及膀胱等器官的肿瘤也是女性多于男性。肺癌、食管癌、肝癌、胃癌、鼻咽癌和结肠癌等则以男性为多见。性别上的这种差异,其原因除一部分与女性激素有关外,主要是可能与男女的性染色体的不同和某一性别较多地接受某种致癌因子的作用有关。
年龄在肿瘤的发病上也有一定的意义。一般来说,肿瘤的发生随年龄的增大而增加,这可用体细胞突变累积来解释。而多见于幼儿和儿童的肿瘤,常与遗传性的基因损害有关,如视网膜母细胞瘤、肾母细胞瘤和神经母细胞瘤等。
(3)种族和地理因素:某些肿瘤在不同种族或地区中的发生率有相当大的差别,如欧美国家的乳腺癌年死亡率是日本的4~5倍,而日本的胃癌年死亡率比美国高7倍。在我国广东、四川和香港、新加坡等地广东人中,鼻咽癌相当常见而且发病年龄较轻。这说明肿瘤与种族有一定的关系。但是也有移民材料说明移居美国的华侨和日侨中,胃癌的发生率在第三代已有明显的下降。因此地理和生活习惯可能也起到一定的作用。
综上所述,随着分子生物学的发展,近年来对于肿瘤的病因与发病机制的研究有了很大的进展。但是肿瘤的发生发展是异常复杂的,目前了解的只是一角,还有许多未知的领域。但以下几点是迄今比较肯定的:①肿瘤从遗传学上的角度上来说是一种基因病。②肿瘤的形成是瘤细胞单克隆性扩增的结果。③环境的和遗传的致癌因素引起的细胞遗传物质(DNA)改变的主要靶基因是原癌基因和和肿瘤抑制基因。原癌基因的激活和(或)肿瘤抑制基因的失活可导致细胞的恶性转化。④肿瘤的发生不只是单个基因突变的结果,而是一个长期的、分阶段的、多种基因突变积累的过程。⑤机体的免疫监视体系在防止肿瘤发生上起重要作用,肿瘤的发生是免疫监视功能丧失的结果。
