室内质量控制系各实验室为了监测和评价本室工作质量,以决定常规检验报告能否发出所采取的一系列检查、控制手段,包括实验室工作的全过程,旨在检测和控制本室常规工作的精密度,并检测其准确度的改变,提高本室常规工作中批间和日间标本检测的一致性,室内质量控制的内容。见表21-1,本节主要介绍分析后的质控知识,其它内容参见有关章节。
表21-1 室内质量控制内容
| 分析前的质控 | 分析中的质控 | 分析后的质控 |
| 病人准备 | 量具与测量 | 计算结果 |
| 标志收集 | 试剂质量 | 标准曲线 |
| 标本处理 | 反应条件 | 控制图绘制 |
| 标本贮存与转运 | 比色测定 | 结果统计分析 |
一、控制物的种类及其使用
控制物是一个广义名词,它包括标准控制物溶液及控制血清等,目前国内外主要使用未定值的控制血清,随常规标本做室内质控。
(一)控制血清的种类
⒈液态控制血清 有动物血和人血制备的控制血清。目前液态控制血清多为实验室自己制备,其中各种成分的含量经实验室多次测定后确定。
⒉冻干控制血清 多由动物血清(猪、牛、马等)制备,分定值与未定值两种。未定值控制血清多用于室内质控,其成分含量由该实验室多次测定后确定。定值血清多由厂家测定或由邀请某些设备及技术水平较好的实验室协助共同测定,此种血清多供室内核对数值使用。
⒊参考血清 其成分经几种参考方法测定。用冻干血清时其瓶间变异小于0.25%,一般是先经透析,除去某些成分,再加入已知量的所需纯品。可用于校正仪器及评价试验方法。
(二)使用控制血清注意事项
⒈使用自制冰冻血清 分装后应注意冰冻保存或低温-10℃~-20℃。如果在一天内连续使用,应注意加盖,避免蒸发。液体血清的优点是不存在分装的问题。但液体血清容易发生细菌污染,细菌污染会改变许多生化成分。
⒉使用冰冻混合血清 由低温情况下取出后,应放置使全溶解,注意混匀后再使用。
⒊使用冻干血清 应严格按照说明书规定操作,注意冻干血清的均一性。即各瓶间差异应在允许范围内,如有怀疑,可随机抽取二三瓶互作测定,观察瓶间差异。如怀疑血清变质或不能较长时间保存,投入使用前应做稳定性试验。一般采用-10或-20℃,室温及37℃三种温度保存,连续定期做测定,将所得数值做比较,观察差异情况。
⒋定值及定限问题 目前均有市售定值控制血清供应。用户往往容易盲目采用产品商所给的数值,但各实验室所用的实验方法不同,因此,在使用前,还应作校对。
二、室内质量控制的主要方法
(一)常规质控图(X-S图)
X-S图法由于它只需要单一浓度的未定值血清,绘图方法简单易懂,有较为成熟的理论和实际经验。因此,成为国内外目前采用最广泛的一种常规室内质量控制方法。一般步骤和具体做法如下:
⒈最佳条件和常规条件下的变异的测定及计算 选择含量均匀、稳定性良好的未定值质控血清,在“最佳条件”,对该批血清反复测定(至少20份),计算出20个结果的X、S和CV,此CV即为最佳条件下的变异(optimalcondition variance,OCV)。取测过OCV的质量控制血清,每天随病人标本测定一瓶,20天后,计算X、S和CV,此CV即为常规条件下的变异(routinecondition variance,RCV)。OCV的测定方法是日间、批间或批内进行,尚无统一意见。但应在尽可能保证最佳条件的前提下,使OCV与RCV有较好的对应性。以便在室内质量控制工作中作对比分析。因此,可每天作4、5批测定,每批测一瓶血清,这样在4、5天内即可得到20个数值,所测得的OCV综合表达了批间和日间精密度。RCV是常规条件下日间精密度的表达指标,因此,测定时必须保证和标本同样的处理条件,而且每天要重新打开一瓶,并只测一份,20个数据要来自20天测定。在测定过程中,如有特殊情况发生,应做详细记录,并将该数据删除,补做一个数据。求出X、S和CV之后,应观察有无超出X±3S范围的数据,在OCV测定中,如有某个数据超出X±3S范围,则应废除全部数据,重新测定OCV。在RCV测定中,有一个数据超出X±3S范围,则删除此数据,用剩余的19个数据计算RCV:如有一个以上数据超出X±3S范围,则应废除该批数据,重新测定RCV。计算结果:通常RCV比OCV大,但一般不超过2倍。且对同一批号质量控制血清OCV和RCV测定中所得X应十分一致,否则应查找原因。OCV过大,往往提示检测方法本身有问题,或测定时未处于最佳条件。RCV过大,则说明常规工作中控制过松,没有达到应有的精密度水平,或由于检测方法不够稳定,难于掌握。
⒉OCV和RCV图的绘制 OCV和RCV的作图十分相似,当使用全国统一印发的质控图纸时,基本步骤如下:
⑴在纵坐标上标出X、X+2S、X-2S、X+3S、X-3S的标志,并将其具体值标在左侧标尺上。
⑵用红笔画出X±2S,用蓝笔画出X±3S线:即成为一张OCV(或RCV)的“空图”。还应填齐图纸上方的各项,如测定项目,测定单位,血清来源及批号,起止日期,主要仪器及使用波长等。测定过程中的特殊情况应在备注栏内记录。
⑶在图纸下方“日期”、“测定值”和“操作者”栏内按原始记录填入相应内容,边填写边核对:注意数据顺序,应严格按实际操作情况,不得颠倒。日期一栏内,在OCV测定中,应改为检测批次(或序号)。在RCV测定中应改为填写实际日期,未做测定的节假日、星期天在图上做出空格似更为合理。因为这样可以真实反映客观情况,便于分析误差原因。
⑷画出每个检测值所对应的图点:每个图点在图上的横坐标为其日期(或序号)而纵坐标(即与X轴相距的小格数目)可按下式计算:

计算结果为正数,则点在X轴上方,反之,则点在X轴下方。各点均画在图上后,用直线将各点顺序连接,以便于观察。OCV和RCV图中各点应呈正态分布,如失去正态分布特点。应进行分析。
⒊X-S图在常规工作质量控制中的应用
⑴按本节前面介绍的RCV“空图”绘制方法:在每个月第一天根据所要用的质量控制血清在RCV测定中所得的X、S绘制一张“空图”。图中X线为靶直线,X±2S线为警告线,X±3S为失控线。
⑵每天将该批号质量控制血清按有关规定复溶(液体的血清则融化),随同各项目病人标本的测定同时测定一份:并按上述方法画出图上的对应点,用直线将该点与前一天的点连接。如果点在X±3S线以外,则为失控。应立即报告有关负责人,迅速查找原因,必要时复测标本,然后才可发出化验报告,并应对失控情况查找的过程及结果处理等详细记录。如果点在X±2S线以外,或出现连续5点以上在X一侧等规律性变化,均应及时向有关负责人反映,并积极查找原因。但当天的化验报告一般可以发出。
⑶月底计算当月全部质量控制血清检测结果的X、S和CV,并进行图形分析和小结,将质量控制图存入质量控制资料档案。
⒋X-S图失控的表现及其处理(图21-1)
⑴测定值的分布规律:按统计学规律,控制血清的数值应依据下列规律分布:①95%的结果应落在X±2S范围内。②有5%的结果可在X±2S外,但在X±3S内;③均值两侧的数据分布几乎相同,不能有连续5次结果在均值的同一侧,或5次数值渐升或渐降,不能有连续有2次结果在X±2S以外;④没有数值落在X±3S以外,结果违反上述规律时,称为失控。
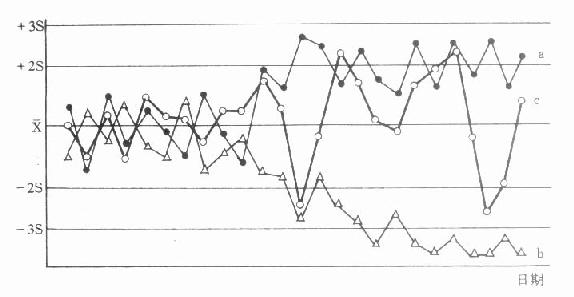
图21-1 X-S质控图的几种失控表现
a.曲线发生漂移;b.曲线趋势性变化;c.曲线精密度出现变化
⑵质控图的几种失控表现:①曲线漂移:“漂移”现象提示存在系统误差,准确度发生了一次性的向上或向下的改变。这种变化往往是由于一个突然出现的新的情况引起的。如更换标准品的生产厂家及批号;重新配制试剂及操作人员的变换等。在寻找原因时,应重点注意“漂移”现象的前后发生了哪些变动因素(图21-1a)。②趋势性变化:向上或向下的趋势性变化,表明检测的准确度发生了逐渐的变化(图21-1b)。这种变化往往是由于一个逐渐改变的因素造成的,如试剂的挥发、吸水、沉淀析出、分光光度计的波长渐渐偏移、光电池老化及质控血清本身的变质等。而更换标准品、试剂或操作者等一次性变化的因素则不大可能造成趋势性变化。③精密度的变化:指常规测定中出现日间差异较大的情况(图21-1c)。从图21-1中可见准确性无明显变化,但精密度从第26天起开始发生变化。
⑶失控后的处理:一般可按以下步骤处理:①迅速回顾、检查整个操作过程,是否有发生错误的环节,如计算错误、吸管及波长选择是否用错等。②如操作步骤均无问题,可重复试验一次,如有改进,说明误差很可能为操作错误所致,如加标本量或试剂量的错误,波长或滤光片选择的错误等偶然误差所致。③如重作后仍不能更正,可取一份新鲜的控制血清重作,观察是否能更正;④如仍不能解决问题,取一份定值血清,用同样方法测定,如结果良好,可能为原血清变质。⑤如仍未得到更正,应仔细检查仪器的各种性能是否正常。⑥如仍未得到纠正,应重新配制试剂或标准液,重新在操作中查找原因。
(二)改良Monica质控图
改良Monica质控图用于室内常规项目的质控,能同时监测精密度和准确度,及时指示存在的误差大小和性质,制作简便,应用及时,形象直观,能将室内质控和室间质评有机地直接联系起来,从质控图上就可基本预测参加室间质评的变异指数得分情况。
⒈Monica质控图绘制
⑴用质量可靠的定值质控血清的测定结果绘图。
⑵该图与X-S图基本相似。其模式如图21-2,在纵轴居中绘出平行于横轴的靶值(target value,T)线,并绘出上下警告值线(warning line)和最大允许值线(max error)4条平行于靶值线的直线。警告值线和最大允许值线用一定范围的选定的变异系数(chosen coefficient variation,CCV)来确定。
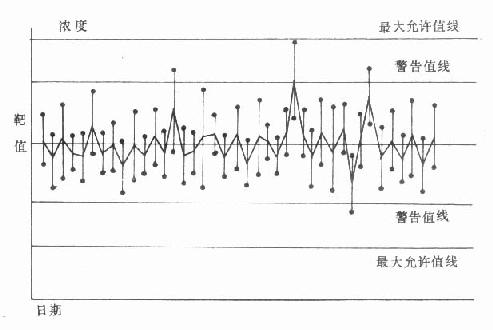
图21-2 Monica质控图模式图
⑶分别以T±0.8CCV×T和T±1.5CCV×T作为警告值和最大允许值。例如:定值质控血清的氯的靶值为115mmol/L,CCV=2.2%,则警告值定为115±0.8×2.2%×115,即113.0-117.0mmol/L,最大允许值定为115±1.5×2.2%×15,即111.2-118.8mmol/L。
在临床生化常规项目的室内质控中,制作Monica质控图时,采用0.8CCV和1.5CCV作为误差界限的目的是试图将室内质控和室间质评更为有机地直接联系起来。根据变异指数(Variance Index,VI)的计算公式:
VI=〔(|X-T|)×100/T〕×100/CCV
式中(|X-T|)/T是测定值的相对误差,用d表示,则:VI=d×100/CCV,若设定VI=80时,则d=0.8CCV。
因此,对一个测定结果,当VI≤80时,则d≤0.8CCV;当80<VI≤150时,则0.8CCV<d≤1.5CCV;当VI>150时,则d<1.5CCV;同理,当d≤0.8CCV时,则VI≤80,即测定结果的相对误差不大于0.8CCV时,VI值也不会大于80,则VIS也不会大于80,在室间质评中成绩为优秀;当0.8CCV<d≤1.5CCV时,则80<VI≤150,即测定结果的相对误差不大于1.5CCV时,VIS也不会大于150,在室间质评中为及格;如果d>1.5CCV,则VI>150,即测定结果的相对误差大于1.5CCV时,VIS就在150以上。在室间质评中不及格。
由此可见,用Monica质控图进行室内质控,如能做到全部测定结果落在警告线内,参加室间质评可获得优秀成绩;如果有些点子分布在警告线外,但在最大允许线内,参加室间质评可望及格;如果经瓽出现超出最大允许线的点子,参加室间质评很难达到及格。
⑷在进行病人标本常规测定中,插入两份质控血清同时操作。将此两个测定值点在质控图上,用垂线将此两点连接,再用红点标出垂线的中点(代表双份测定的均值),然后用细线将相邻的红点连起来见图21-2。
⒉结果分析与判断标准 按照Monica原判断标准,最理想的结果是质控血清的全部测定值(不是双份测定的均值)都落在警告线内。如果超出警告线,但仍在最大允许线内,该批病人标本测定结果仍然有效,即“在控”,但指示测定误差较大,须仔细检查可能产生误差的各个环节。出现任何落在最大允许线外的点都表示“失控”,该批测定结果无效,应查明误差原因并予消除后重新测定。
在Monica质控图中,由于相邻各红点连线与X-S质控图相似,因此,X-S质控图的分析判断标准也基本适用Monica质控图。
在Monica质控图中,双份重复测定值的垂线的长短可作为精密度的指示,愈短精密度愈好,愈长则愈差。红点离靶值线的远近可作为准确度的指示,离得愈近,准确度愈好,愈远则愈差。可根据垂线的长短和红点的位置,分析判断该批测定结果的精密度和准确度及其误差的大小和性质。
⒊Monica质控图的优点
⑴制作简单,应用方便:只要有质量可靠的定值质控血清,就可立即制图应用。而X-S质控图需进行20天定值确定X与S后方可绘图。
⑵Monica质控图与X-S质控图很相似:只是使用定值质控血清,作双份重复测定,用双份测定值的垂直线的长短来监测偶然误差,用垂线中点的位置来监测准确度,既形象直观,又容易理解和掌握。
⑶Monica质控图采用统一CCV作为允许误差来确定警告线和最大允许线的界限值,能将临床生化常规项目的室内质控与室间质评有机地联系起来:从室内质控图上,既可基本预测参加室间质评可能获得的变异指数得分情况,更能充分发挥室内质控与室间质评二者之间相互补充,相互促进的作用。
除以上介绍的两种室内质控方法外,尚有均数和范围质控图,累加与质控图和病人标本测定结果均值图等,一般应用较少,必要时参考有关文献。
