蛋白质为生物高分子物质之一,具有三维空间结构,因而执行复杂的生物学功能。蛋白质结构与功能之间的关系非常密切。在研究中,一般将蛋白质分子的结构分为一级结构与空间结构两类。
一、蛋白质的一级结构
蛋白质的一级结构(primarystructure)就是蛋白质多肽链中氨基酸残基的排列顺序(sequence),也是蛋白质最基本的结构。它是由基因上遗传密码的排列顺序所决定的。各种氨基酸按遗传密码的顺序,通过肽键连接起来,成为多肽链,故肽键是蛋白质结构中的主键。
迄今已有约一千种左右蛋白质的一级结构被研究确定,如胰岛素,胰核糖核酸酶、胰蛋白酶等。
蛋白质的一级结构决定了蛋白质的二级、三级等高级结构,成百亿的天然蛋白质各有其特殊的生物学活性,决定每一种蛋白质的生物学活性的结构特点,首先在于其肽链的氨基酸序列,由于组成蛋白质的20种氨基酸各具特殊的侧链,侧链基团的理化性质和空间排布各不相同,当它们按照不同的序列关系组合时,就可形成多种多样的空间结构和不同生物学活性的蛋白质分子。
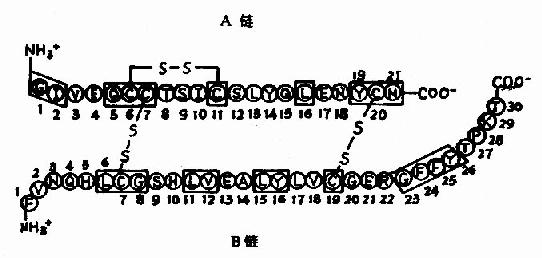
图1-1 胰岛素的一级结构
二、蛋白质的空间结构
蛋白质分子的多肽链并非呈线形伸展,而是折叠和盘曲构成特有的比较稳定的空间结构。蛋白质的生物学活性和理化性质主要决定于空间结构的完整,因此仅仅测定蛋白质分子的氨基酸组成和它们的排列顺序并不能完全了解蛋白质分子的生物学活性和理化性质。例如球状蛋白质(多见于血浆中的白蛋白、球蛋白、血红蛋白和酶等)和纤维状蛋白质(角蛋白、胶原蛋白、肌凝蛋白、纤维蛋白等),前者溶于水,后者不溶于水,显而易见,此种性质不能仅用蛋白质的一级结构的氨基酸排列顺序来解释。
蛋白质的空间结构就是指蛋白质的二级、三级和四级结构。
(一)蛋白质的二级结构
蛋白质的二级结构(secondarystructure)是指多肽链中主链原子的局部空间排布即构象,不涉及侧链部分的构象。
1.肽键平面(或称酰胺平面,amide plane)。
Pauling等人对一些简单的肽及氨基酸的酰胺等进行了X线衍射分析,得出图1-2所示结构,从一个肽键的周围来看,得知:
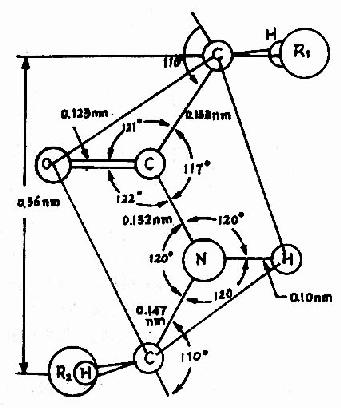
图1-2 肽键平面示意图
(1)
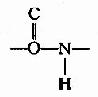
中的C-N键长0.132nm,比相邻的N-C单键(0.147nm)短,而较一般C=N双键(0.128nm)长,可见,肽键中-C-N-键的性质介于单、双键之间,具有部分双键的性质,因而不能旋转,这就将固定在一个平面之内。
(2)
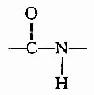
肽键的C及N周围三个键角之和均为360°,说明都处于一个平面上,也就是说
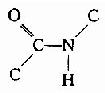
六个原子基本上同处于一个平面,这就是肽键平面。肽链中能够旋转的只有α碳原子所形成的单键,此单键的旋转决定两个肽键平面的位置关系,于是肽键平面成为肽链盘曲折叠的基本单位。
(3) 肽键中的C-N既具有双键性质,就会有顺反不同的立体异构,已证实
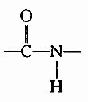
处于反位(见图1-3)。
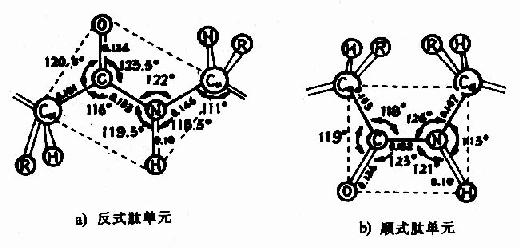
图1-3 反式肽单元和顺式肽单元
2.蛋白质主链构象的结构单元
1)α-螺旋Pauling等人对α-角蛋白(α-keratin)进行了X线衍射分析,从衍射图中看到有0.5~0.55nm的重复单位,故推测蛋白质分子中有重复性结构,并认为这种重复性结构为α-螺旋(α-helix)见图1-4。
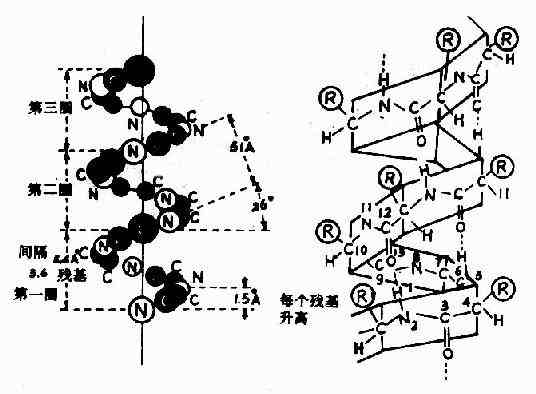
图1-4 蛋白质分子的α-螺旋
α-螺旋的结构特点如下:
(1)多个肽键平面通过α-碳原子旋转,相互之间紧密盘曲成稳固的右手螺旋。
(2)主链呈螺旋上升,每3.6个氨基酸残基上升一圈,相当于0.54nm,这与X线衍射图符合。
(3)相邻两圈螺旋之间借肽键中C=O和H桸形成许多链内氢健,即每一个氨基酸残基中的NH和前面相隔三个残基的C=O之间形成氢键,这是稳定α-螺旋的主要键。
(4)肽链中氨基酸侧链R,分布在螺旋外侧,其形状、大小及电荷影响α-螺旋的形成。酸性或碱性氨基酸集中的区域,由于同电荷相斥,不利于α-螺旋形成;较大的R(如苯丙氨酸、色氨酸、异亮氨酸)集中的区域,也妨碍α-螺旋形成;脯氨酸因其α-碳原子位于五元环上,不易扭转,加之它是亚氨基酸,不易形成氢键,故不易形成上述α-螺旋;甘氨酸的R基为H,空间占位很小,也会影响该处螺旋的稳定。
2)β-片层结构Astbury等人曾对β-角蛋白进行X线衍射分析,发现具有0.7nm的重复单位。如将毛发α-角蛋白在湿热条件下拉伸,可拉长到原长二倍,这种α-螺旋的X线衍射图可改变为与β-角蛋白类似的衍射图。说明β-角蛋白中的结构和α-螺旋拉长伸展后结构相同。两段以上的这种折叠成锯齿状的肽链,通过氢键相连而平行成片层状的结构称为β-片层(β-pleatedsheet)结构或称β-折迭(图1-5)。
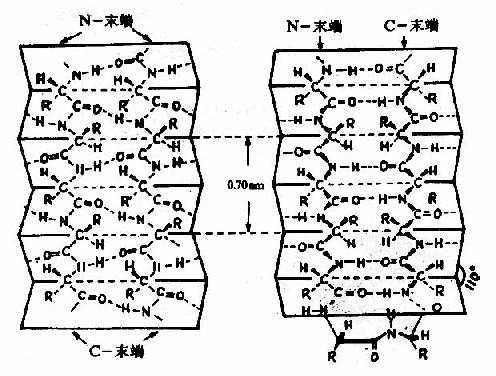
图1-5 蛋白质分子中的β-片层结构
左:顺向平行 右:逆向平行
β-片层结构特点是:
①是肽链相当伸展的结构,肽链平面之间折叠成锯齿状,相邻肽键平面间呈110°角。氨基酸残基的R侧链伸出在锯齿的上方或下方。
②依靠两条肽链或一条肽链内的两段肽链间的C=O与H梄形成氢键,使构象稳定。
③两段肽链可以是平行的,也可以是反平行的。即前者两条链从“N端”到“C端”是同方向的,后者是反方向的。β-片层结构的形式十分多样,正、反平行能相互交替。
④平行的β-片层结构中,两个残基的间距为0.65nm;反平行的β-片层结构,则间距为0.7nm。
3)β-转角
蛋白质分子中,肽链经常会出现180°的回折,在这种回折角处的构象就是β-转角(β-turn或β-bend)。β-转角中,第一个氨基酸残基的C=O与第四个残基的N桯形成氢键,从而使结构稳定(图1-6)。
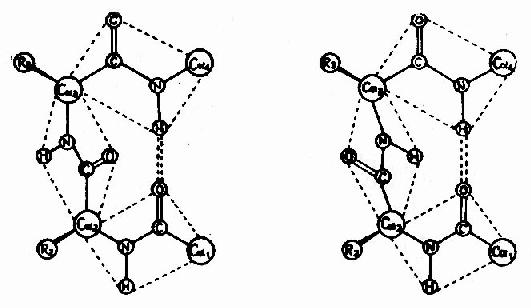
图1-6 蛋白质分子中的β-转角
4)无规卷曲
没有确定规律性的部分肽链构象,肽链中肽键平面不规则排列,属于松散的无规卷曲(random coil)。
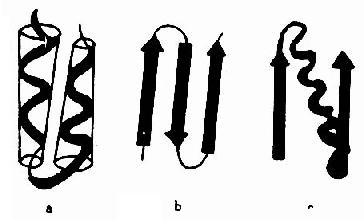
图1-7 蛋白质的超二级结构示意
a.αα组合 b.βββ组合 c.βαβ组合
(二)超二级结构和结构域
超二级结构(supersecondarystructure)是指在多肽链内顺序上相互邻近的二级结构常常在空间折叠中靠近,彼此相互作用,形成规则的二级结构聚集体。目前发现的超二级结构有三种基本形式:α螺旋组合(αα);β折叠组合(βββ)和α螺旋β折叠组合(βαβ)(图1-7),其中以βαβ组合最为常见。它们可直接作为三级结构的“建筑块”或结构域的组成单位,是蛋白质构象中二级结构与三级结构之间的一个层次,故称超二级结构。
结构域(domain)也是蛋白质构象中二级结构与三级结构之间的一个层次。在较大的蛋白质分子中,由于多肽链上相邻的超二级结构紧密联系,形成二个或多个在空间上可以明显区别它与蛋白质亚基结构的区别。一般每个结构域约由100-200个氨基酸残基组成,各有独特的空间构象,并承担不同的生物学功能。如免疫球蛋白(IgG)由12个结构域组成,其中两个轻链上各有2个,两个重链上各有4个;补体结合部位与抗原结合部位处于不同的结构域。一个蛋白质分子中的几个结构域有的相同,有的不同;而不同蛋白质分子之间肽链中的各结构域也可以相同。如乳酸脱氢酶、3-磷酸甘油醛脱氢酶、苹果酸脱氢酶等均属以NAD+为辅酶的脱氢酶类,它们各自由2个不同的结构域组成,但它们与NAD+结合的结构域构象则基本相同。
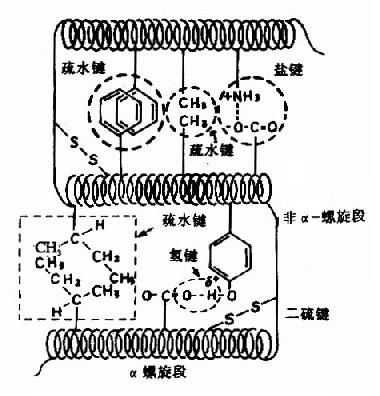
图1-8 蛋白质三级结构中某些次级键
(三)蛋白质的三级结构
蛋白质的多肽链在各种二级结构的基础上再进一步盘曲或折迭形成具有一定规律的三维空间结构,称为蛋白质的三级结构(tertiary structure)。蛋白质三级结构的稳定主要靠次级键,包括氢键、疏水键、盐键以及范德华力(Van der Wasls力)等(图1-8)。这些次级键可存在于一级结构序号相隔很远的氨基酸残基的R基团之间,因此蛋白质的三级结构主要指氨基酸残基的侧链间的结合。次级键都是非共价键,易受环境中pH、温度、离子强度等的影响,有变动的可能性。二硫键不属于次级键,但在某些肽链中能使远隔的二个肽段联系在一起,这对于蛋白质三级结构的稳定上起着重要作用。
现也有认为蛋白质的三级结构是指蛋白质分子主链折叠盘曲形成构象的基础上,分子中的各个侧链所形成一定的构象。侧链构象主要是形成微区(或称结构域domain)。对球状蛋白质来说,形成疏水区和亲水区。亲水区多在蛋白质分子表面,由很多亲水侧链组成。疏水区多在分子内部,由疏水侧链集中构成,疏水区常形成一些“洞穴”或“口袋”,某些辅基就镶嵌其中,成为活性部位。
具备三级结构的蛋白质从其外形上看,有的细长(长轴比短轴大10倍以上),属于纤维状蛋白质(fibrous protein),如丝心蛋白;有的长短轴相差不多基本上呈球形,属于球状蛋白质(globular protein),如血浆清蛋白、球蛋白、肌红蛋白,球状蛋白的疏水基多聚集在分子的内部,而亲水基则多分布在分子表面,因而球状蛋白质是亲水的,更重要的是,多肽链经过如此盘曲后,可形成某些发挥生物学功能的特定区域,例如酶的活性中心等。
(四)蛋白质的四级结构
具有二条或二条以上独立三级结构的多肽链组成的蛋白质,其多肽链间通过次级键相互组合而形成的空间结构称为蛋白质的四级结构(quarternary structure)。其中,每个具有独立三级结构的多肽链单位称为亚基(subunit)。四级结构实际上是指亚基的立体排布、相互作用及接触部位的布局。亚基之间不含共价键,亚基间次级键的结合比二、三级结构疏松,因此在一定的条件下,四级结构的蛋白质可分离为其组成的亚基,而亚基本身构象仍可不变。
一种蛋白质中,亚基结构可以相同,也可不同。如烟草斑纹病毒的外壳蛋白是由2200个相同的亚基形成的多聚体;正常人血红蛋白A是两个α亚基与两个β亚基形成的四聚体;天冬氨酸氨甲酰基转移酶由六个调节亚基与六个催化亚基组成。有人将具有全套不同亚基的最小单位称为原聚体(protomer),如一个催化亚基与一个调节亚基结合成天冬氨酸氨甲酰基转移酶的原聚体。
某些蛋白质分子可进一步聚合成聚合体(polymer)。聚合体中的重复单位称为单体(monomer),聚合体可按其中所含单体的数量不同而分为二聚体、三聚体……寡聚体(oligomer)和多聚体(polymer)而存在,如胰岛素(insulin)在体内可形成二聚体及六聚体。
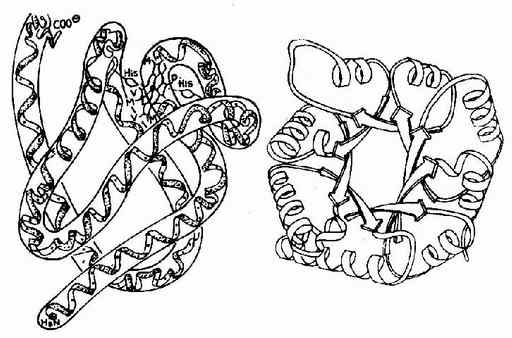
图1-9 肌红蛋白的三级结构和丙糖磷酸异构酶的三级结构图
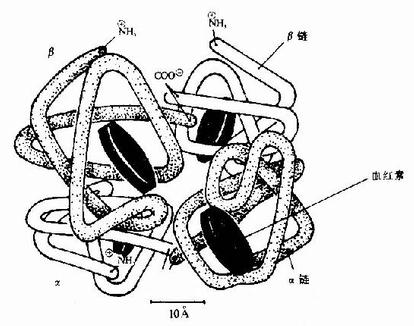
图1-10 面红蛋白亚基结合模式图
三、蛋白质的结构与功能的关系
(一)蛋白质的一级结构与其构象及功能的关系
蛋白质一级结构是空间结构的基础,特定的空间构象主要是由蛋白质分子中肽链和侧链R基团形成的次级键来维持,在生物体内,蛋白质的多肽链一旦被合成后,即可根据一级结构的特点自然折叠和盘曲,形成一定的空间构象。
Anfinsen以一条肽链的蛋白质核糖核酸酶为对象,研究二硫键的还原和氧化问题,发现该酶的124个氨基酸残基构成的多肽链中存在四对二硫键,在大量β-巯基乙醇和适量尿素作用下,四对二硫键全部被还原为桽H,酶活力也全部丧失,但是如将尿素和β-巯基乙醇除去,并在有氧条件下使巯基缓慢氧化成二硫键,此时酶的活力水平可接近于天然的酶。Anfinsen在此基础上认为蛋白质的一级结构决定了它的二级、三级结构,即由一级结构可以自动地发展到二、三级结构(图1-10)。
一级结构相似的蛋白质,其基本构象及功能也相似,例如,不同种属的生物体分离出来的同一功能的蛋白质,其一级结构只有极少的差别,而且在系统发生上进化位置相距愈近的差异愈小(表1-2,表1-3)。
表1-2 胰岛素分子中氨基酸残基的差异部分
| 胰岛素来源 | 氨基酸残基的差异部分 | |||
| A5 | A6 | A10 | A30 | |
| 人 | Thr | Ser | Ile | Thr |
| 猪 | Thr | Ser | Ile | Ala |
| 狗 | Thr | Ser | Ile | Ala |
| 兔 | Thr | Ser | Ile | Ser |
| 牛 | Ala | Ser | Val | Ala |
| 羊 | Ala | Gly | Val | Ala |
| 马 | Thr | Gly | Ile | Ala |
| 抹香猄 | Thr | Ser | Ile | Ala |
| 鲤猄 | Ala | Ser | Thr | Ala |
表1-3 细胞色素C分子中氨基酸残基的差异数目及分歧时间
| 不同种属 | 氨基酸残基的差异数目 | 分歧时间(百万年) |
| 人-猴 | 1 | 50-60 |
| 人-马 | 12 | 70-75 |
| 人-狗 | 10 | 70-75 |
| 猪-牛-羊 | 0 | |
| 马-牛 | 3 | 60-65 |
| 哺乳类-鸡 | 10-15 | 280 |
| 哺乳类-猢 | 17-21 | 400 |
| 脊椎动物-酵母 | 43-48 | 1,100 |
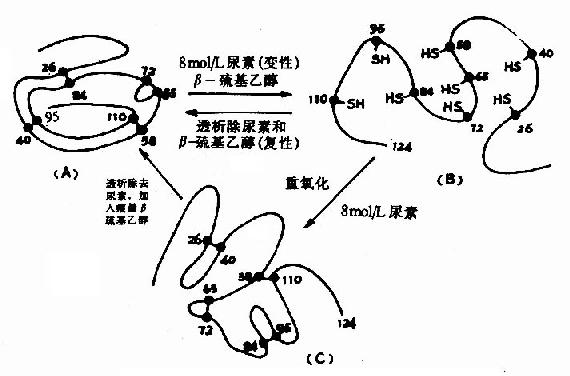
图1-11 核糖核酸酶的变性和复性示意图
(A)天然核糖核酸酶(B)变性失活(C)“错乱”核糖核酸酶
促肾上腺皮质激素(ACTH)和促黑激素(MSH)均为垂体分泌的多肽激素。α-MSH和ACTh 4~10位的氨基酸结构与β-MSH的11~17位一样,故ACTH有较弱的MSH的生理作用(图1-12)。
在蛋白质的一级结构中,参与功能活性部位的残基或处于特定构象关键部位的残基,即使在整个分子中发生一个残基的异常,那么该蛋白质的功能也会受到明显的影响。被称之为“分子病”的镰刀状红细胞性贫血仅仅是574个氨基酸残基中,一个氨基酸残基即β亚基N端的第6号氨基酸残基发生了变异所造成的,这种变异来源于基因上遗传信息的突变(如图1-13)。
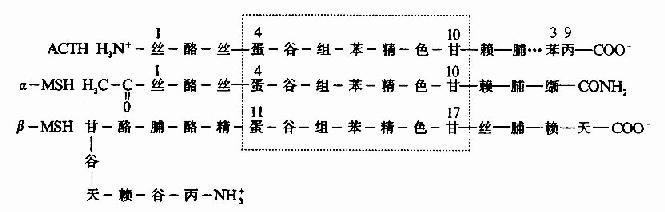
图1-12 ACTH、α-MSH和β-MSH一级结构比较
| 正常 | DNA | ……TGt GGG CTT CTT TTT…… |
| mRNA | ACA CCC GAA GAA AAA | |
| DNA(β亚基) | N端…苏-脯-谷-谷-赖…… | |
| 异常 | DNA | ……TGT GGG GAT CTT TTT…… |
| mRNA | ……ACa CCC GUA GAA AAA…… | |
| hbs(β亚基) | N端…苏-脯-缬-谷-赖…… |
图1-13 镰刀状红细胞性贫血血红蛋白遗传信息的异常
(二)蛋白质空间橡象与功能活性的关系
蛋白质多种多样的功能与各种蛋白质特定的空间构象密切相关,蛋白质的空间构象是其功能活性的基础,构象发生变化,其功能活性也随之改变。蛋白质变性时,由于其空间构象被破坏,故引起功能活性丧失,变性蛋白质在复性后,构象复原,活性即能恢复。
在生物体内,当某种物质特异地与蛋白质分子的某个部位结合,触发该蛋白质的构象发生一定变化,从而导致其功能活性的变化,这种现象称为蛋白质的别构效应(allostery)。
蛋白质(或酶)的别构效应,在生物体内普遍存在,这对物质代谢的调节和某些生理功能的变化都是十分重要的。
现以血红蛋白(hemoglobin,简写Hb)为例来说明构象与功能的关系。
血红蛋白是红细胞中所含有的一种结合蛋白质,它的蛋白质部分称为珠蛋白(globin),非蛋白质部分(辅基)称为血红素(见图1-14)。Hb分子由四个亚基构成,每一亚基结合一分子血红素。正常成人Hb分子的四个亚基为两条α链,两条β链。α链由141个氨基酸残基组成,β链由146个氨基酸残基组成,它们的一级结构均已确定。每一亚基都具有独立的三级结构,各肽链折叠盘曲成一定构象,β亚基中有8个α-螺旋区(分别称A、B……H螺旋区),α亚基中有7个α-螺旋区。在此基础上肽链进一步折叠形成球状,依赖侧链间形成的各种次级键维持稳定,使之球形表面为亲水区,球形向内,在E和F螺旋段间的20多个巯水氨基酸侧链构成口袋形的疏水区,辅基血红素就嵌接在其中,α亚基和β亚基构象相似,最后,四个亚基α2β2聚合成具有四级结构的Hb分子(见图1-15)。在此分子中,四个亚基沿中央轴排布四方,两α亚基沿不同方向嵌入两个β亚基间,各亚基间依多种次级健联系,使整个分子呈球形,这些次级键对于维系Hb分子空间构象有重要作用,例如在四亚基间的8对盐键(图1-16),它们的形成和断裂将使整个分子的空间构象发生变化。
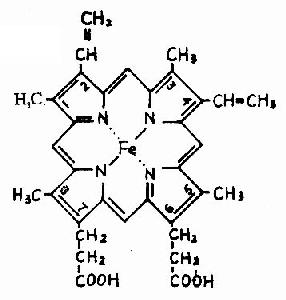
图1-14 血红素的结构式
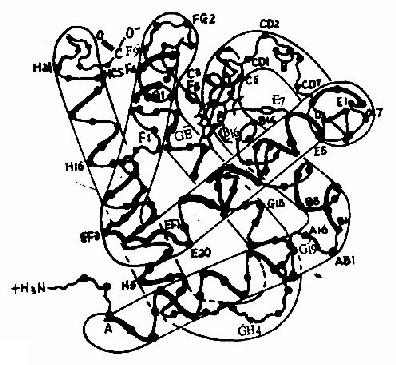
图1-15 血红蛋白β亚基的构象
ABCDEFGH分别代表不同的α-螺旋区。共有八个螺旋区;阿拉伯数字代表在该区氨基酸残基的序号;a-螺旋区之间的移行部位为无规卷曲,用AB,CD,EF,FG…等表示。C1,E7,C5,CF,C3,E3,的中间为血红素,其中较大的黑点代表Fe2+。
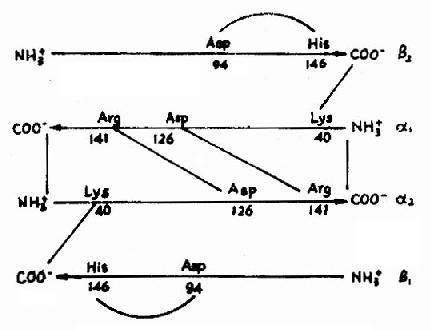
图1-16 血红蛋白亚基间盐键示意图
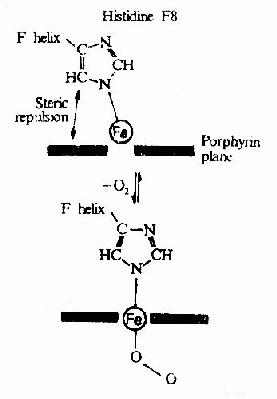
图1-7 铁原子在氧合时落入血红素平面
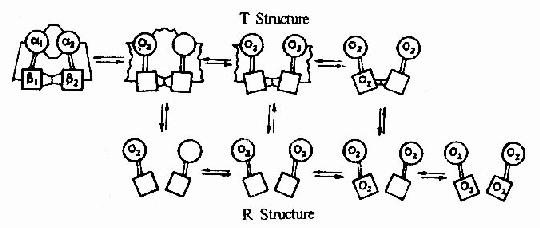
图1-18
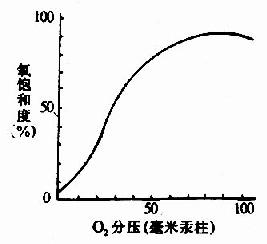
图1-19 Hb的氧饱和曲线
Hb在体内的主要功能为运输氧气,而Hb的别位效应,极有利于它在肺部与O2结合及在周围组织释放O2。
Hb是通过其辅基血红素的Fe++与氧发生可逆结合的,血红素的铁原子共有6个配位键,其中4个与血红素的吡咯环的N结合,一个与珠蛋白亚基F螺旋区的第8位组氨酸(F8)残基的咪唑基的N相连接,空着的一个配位键可与O2可逆地结合,结合物称氧合血红蛋白。
在血红素中,四个吡咯环形成一个平面,在未与氧结合时Fe++的位置高于平面0.7Å,一旦O2进入某一个α亚基的疏水“口袋”时,与Fe++的结合会使Fe++嵌入四吡咯平面中,也即向该平面内移动约0.75Å(图1-17),铁的位置的这一微小移动,牵动F8组氨酸残基连同F螺旋段的位移,再波及附近肽段构象,造成两个α亚基间盐键断裂,使亚基间结合变松,并促进第二亚基的变构并氧合,后者又促进第三亚基的氧合(图1-18)使Hb分子中第四亚基的氧合速度为第一亚基开始氧合时速度的数百倍。此种一个亚基的别构作用,促进另一亚基变构的现象,称为亚基间的协同效应(cooperativity),所以在不同氧分压下,Hb氧饱和曲线呈“S”型(图1-19)。
